Амиотрофия Вердинга-Гоффмана

Невролог, нейрофизиолог, стаж - 38 лет;
Профессор неврологии, доктор медицинских наук;
Клиника восстановительной неврологии.Об авторе
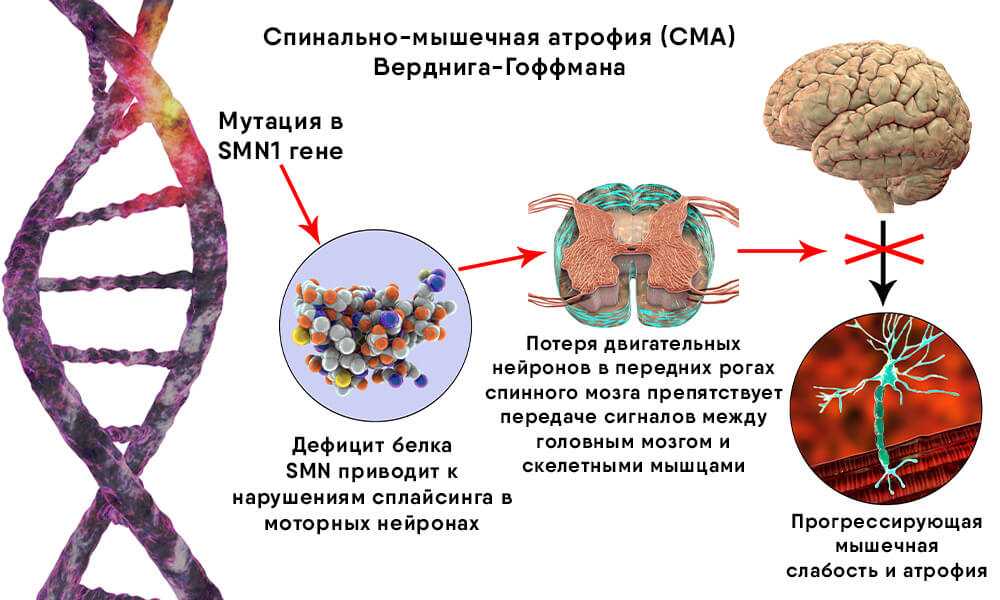
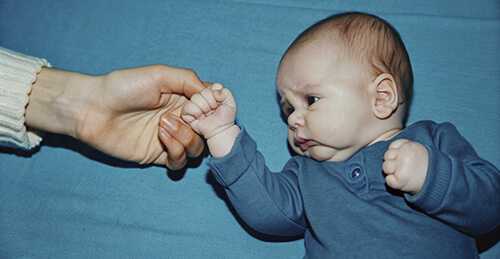
Синдром Вердинга – Гоффмана – это наиболее тяжёлая форма спинальной мышечной атрофии, развивающейся у новорождённых детей в первые месяцы жизни и быстро приводящая к гибели. Это наследственное генетическое заболевание, способное поражать как мальчиков, так и девочек. Болезнь проявляется как быстро прогрессирующие мышечные атрофии, сопровождающиеся парезами, приводящими к полной парализованности человека. [1]
В большинстве случаев спинально-мышечная атрофия Верднига-Гоффмана сочетается с другими тяжёлыми аномалиями развития и деформациями костей различного типа.
Амиотрофия Верднига считается самым тяжёлым вариантом спинально-мышечной атрофии, в очень короткие сроки приводящим к летальному исходу. При этом частота заболевания — 1 случай на 7-10 тысяч рождений в зависимости от развитости медицины в стране.
Работа с детьми с болезнью Гоффмана – это наиболее тяжёлая обязанность неонатологов и педиатров, работающих с младенцами, так как действенное лечение, способное остановить развитие, ещё не разработано.
Несмотря на то что синдром проявляется достаточно редко, носителем поломанного гена, который может привести к развитию болезни, является каждый 50-й человек. Однако передаётся патология только аутосомно-рецессивным типом наследования, что позволяет сильно снизить её частотность. Ребёнок с таким диагнозом родится, только если оба родителя являются носителями мутации. И то вероятность возникновения заболевания будет не выше 25%.
Симптомы
Врождённая форма
Симптомы болезни Верднига-Гоффмана иногда проявляются так рано, что врачи не успевают понять, что это такое до того, как симптоматика сильно разовьётся, тогда ставится диагноз СМА 1 типа.
Манифестирует эта патология развития до того, как малышу исполнится 6 месяцев. Первые признаки появляются ещё в период вынашивания. Плод крайне мало шевелится, матерью практически не ощущаются толчки и смена положения.
В большинстве случаев проблемы с мышцами наблюдаются с первых дней жизни. При этом отмечается, что глубинные рефлексы у таких детей сразу же угасают. Ребёнок не способен освоить первоначальные навыки: не может самостоятельно питаться, поднять голову или начать кричать. Иногда, когда первые проявления болезни начинаются позже, малыш может научиться первым двигательным навыкам: поддерживать голову и переворачиваться, но они очень быстро регрессируют.
Этот тип заболевания не проявляется самостоятельно, чаще всего с ним «сцеплен» ещё ряд нарушений:
- Врождённая олигофрения.
- Дисплазия тазобедренных суставов.
- Косолапость.
- Гидроцефалия.
- Нарушения в формировании костей и суставов: искривление позвоночника, нарушения в развитии грудной клетки.
- Гемангиомы.
Течение СМА 1 типа наиболее тяжёлое и быстрое. Всего за несколько недель из-за нарастающей атрофии мышц появляется обездвиженность, нарушения в работе дыхательной мускулатуры. Невозможность самостоятельно дышать – главная причина наступления смерти при этом диагнозе. Из-за нарушения глотательной функции возможно, что смесь или молоко при попытке кормления забрасывается не в желудок, а в лёгкие.
Ранняя детская форма
СМА 2 типа проявляется в возрасте от полугода до года.
Ребёнок с рождения уже является носителем заболевания, которое временно спит. Включается и манифестирует синдром Вердинга – Гоффмана в таком случае после пищевого отравления или любой перенесённой инфекции. [2]
После пробуждения СМА2 типа постепенно происходит атрофия мышц, начиная с нижних конечностей, угасание глубинных рефлексов. Но на развитие уходит больше времени, чем при 1 типе. При удачном стечении обстоятельств и вовремя начатом поддерживающей терапии есть вероятность, что ребёнок сможет дожить до 15 лет, но большинство пациентов доживают только до 2 – 2,5 лет.
Основными симптомами развития СМА 2 типа являются:
- Снижение активности и потеря силы в ногах.
- Поражение нервной системы, провоцирующее атрофии мышц всего организма.
- Подрагивание пальцев.
- Неконтролируемые движения языка из-за внезапных сокращений мышц.
- Диффузная мышечная гипотония.
- Усиливающиеся проблемы с дыханием вплоть до полного отказа мускулатуры, контролирующей этот процесс.
Амиотрофия Кугельберга-Веландера
Многие учёные выделяют этот тип проявления генной мутации, как отдельную болезнь, так как по проявлениям она сильно отличается от 1 и 2 типа СМА, однако фактически является подвидом именно этой болезни, так как провоцируется той же самой мутацией.
В отличие от 1 и 2 типов, манифестирует впервые после 2 лет, в редких случаях после 15 лет. Развитие патологии идёт значительно медленнее, что позволяет с помощью лечения обеспечить человеку более продолжительную жизнь и возможность некоторой самостоятельности.
Диагностика
Больные с выявленным диагнозом спинальная мышечная атрофия 1 типа должны с рождения оставаться в больнице под постоянным наблюдением специалистов. Крайне важно время манифестации заболевания. Практически всегда, за редким исключением, это происходит от периода рождения и до исполнения полугода. Дополнительным маркером опасности развития генетического заболевания является отметка о малом количестве шевелений на последних неделях развития плода. [3]
Невролог выявляет выраженную мышечную гипотонию, отсутствие развития навыков по возрасту. Малыш не может сесть, удерживать голову или принимать «позу лягушки». Появляются неконтролируемые подёргивания мышц, не появляются сухожильные рефлексы. Невооружённым глазом чаще всего видны значительные деформации рёбер или нижних конечностей.
Чтобы точно подтвердить диагноз, необходимо провести дополнительное обследование с помощью аппаратных методов:
- Игольчатая электронейромиография. При прохождении процедуры фиксируется значительное снижение скорости проведения сигнала по сравнению с нормотипичными показателями, внезапная активность, хотя изначально тело должно находиться в покое.
- Спирометрия. Так как поражение мышц, отвечающих за дыхание и, как следствие, её слабость – главные признаки, то значительное снижение жизненной ёмкости лёгких будет важным фактом, подсказывающим точный диагноз.
- Гистология. При обследовании биоптата, извлечённого из повреждённых мышц, будет определена пучковая атрофия мышечных волокон, перемежающаяся стандартными здоровыми тканями, также обнаружится соединительнотканные возрастания.
- Лабораторные анализы. Исследование химического состава крови. При получении результатов у части пациентов обнаруживается отклонение от нормы в количестве креатинфосфокиназы. Также отличительной чертой является сниженный уровень кислорода и повышенный углекислого газа.
- Генетическое тестирование проводится после остальных исследований, так как его задача – верифицировать диагноз, показать, что генетическая мутация (делеция) SMN1 экзона 7 действительно у пациента есть.
Лечение
Если неонатолог или детский невролог определяет, что болезнь новорождённого малыша – это спинальная мышечная амиотрофия Вердинга-Гоффмана 1 или 2 типа, то пациент немедленно направляется для амбулаторного лечения в стационар специализированной больницы. Сегодня не существует способа избавиться от заболевания, поэтому все применяемые методы и препараты используются для облегчения симптоматики синдрома и паллиативной помощи.
В случае, когда дыхательная мускулатура уже поражена, пациента сразу переводят в реанимационное отделение и используют аппарат ИВЛ.
Для того чтобы продлить жизнь маленького пациента и уменьшить его мучения, используют:
- Медикаментозная терапия. Используются различные группы препаратов, направленные на улучшение метаболизма в мышечных тканях, поддержку работы желудочно-кишечного тракта и органов дыхания.
- Респираторная поддержка. Крайне важно для замедления развития синдрома и смягчения симптомов избавиться от кислородной недостаточности. Поэтому пациенту доставляют дополнительный кислород, используя для этого маску или, если дыхательная мускулатура уже не способна справиться со своей функцией, через аппарат ИВЛ. [4]
- Кормление. Так как рефлексы, необходимые для полноценного питания, быстро пропадают, то процесс кормления ребёнка несколько меняется. В процессе он должен принимать вертикальное положение. Допустимо использование жидкой и полутвёрдой пищи для более взрослых пациентов.
- ЛФК. Для поддержания мышечного тонуса необходимы ежедневные специализированные тренировки пассивного типа. Все движения и упражнения выполняются не самим пациентом, а специалистом.
- Физиотерапия используется для улучшения кровообращения в мышечной ткани. Для этого применяется электрофорез, транскраниальная магнитная стимуляция, вихревые магнитные поля, биорезонанс и другие процедуры.
- Ортопедическое лечение. Чтобы предотвратить деформацию костей и суставов, используются специализированные приспособления.
В редких случаях, при которых пациент имеет возможность прожить дольше нескольких месяцев, но при этом имеет выраженные деформации грудной клетки, позвоночника, выраженные контрактуры суставов, проводятся ортопедические операции. Если пациент страдает частыми пневмониями из-за того, что является лежачим, ему могут провести трахеотомию.
Исследования, посвящённые возможности побороть врождённую генетически обусловленную амиотрофию ведутся в лучших исследовательских университетах мира. На данный момент учёные отдают предпочтение направлению, разрабатывающему возможность исправление мутировавшего гена.
В 2019 году был запатентован и одобрен для клинического применения, в том числе в России, лекарственный препарат Золгенсма. Его функция – увеличить выработку белка SMN1, что сильно улучшит состояние пациентов и замедлит развитие болезни.
Прогноз и профилактика
Синдром Верднига -Хоффмана является генетическим заболеванием, на данном этапе развития медицины неизлечимым. Если она проявляется у пациента, то благоприятного исхода быть не может. Дети, симптомы болезни у которых были выявлены с первых дней жизни, не доживают и до 6 месяцев. Если развитие патологии началось позже, после достижения 3 месяцев, то ребёнок обычно доживает до 2 лет.
Ранняя детская форма, манифестирующая в более позднем возрасте, развивается значительно медленнее и позволяет дожить до 13-14 лет при глубокой инвалидизации. На данный момент лечение способно только облегчить течение болезни и снять некоторые симптомы, но не замедлить её развитие.
Единственным видом вторичной профилактики является избегание осложняющих течение болезни факторов – пневмонии, инфекционных заболеваний нижних дыхательных путей, контрактур суставов.
Список использованной литературы:
- ^ Audic F, Barnerias C. “Spinal muscular atrophy (SMA) type I (Werdnig-Hoffmann disease).” Arch Pediatr. 2020 Dec;27(7S):7S15-7S17. doi: 10.1016/S0929-693X(20)30271-2. PMID: 33357591.
- ^ Borkowska J, Rudnik-Schoneborn S, Hausmanowa-Petrusewicz I, Zerres K. “Early infantile form of spinal muscular atrophy (Werdnig-Hoffmann disease) with prolonged survival.” Folia Neuropathol. 2002;40(1):19-26. PMID: 12121035.
- ^ Mercuri E, Finkel RS, Muntoni F, Wirth B, Montes J, Main M, Mazzone ES, Vitale M, Snyder B, Quijano-Roy S, Bertini E, Davis RH, Meyer OH, Simonds AK, Schroth MK, Graham RJ, Kirschner J, Iannaccone ST, Crawford TO, Woods S, Qian Y, Sejersen T; SMA Care Group. “Diagnosis and management of spinal muscular atrophy: Part 1: Recommendations for diagnosis, rehabilitation, orthopedic and nutritional care.” Neuromuscul Disord. 2018 Feb;28(2):103-115. doi: 10.1016/j.nmd.2017.11.005. Epub 2017 Nov 23. PMID: 29290580.
- ^ Fauroux B, Griffon L, Amaddeo A, Stremler N, Mazenq J, Khirani S, Baravalle-Einaudi M. “Respiratory management of children with spinal muscular atrophy (SMA).” Arch Pediatr. 2020 Dec;27(7S):7S29-7S34. doi: 10.1016/S0929-693X(20)30274-8. PMID: 33357594.